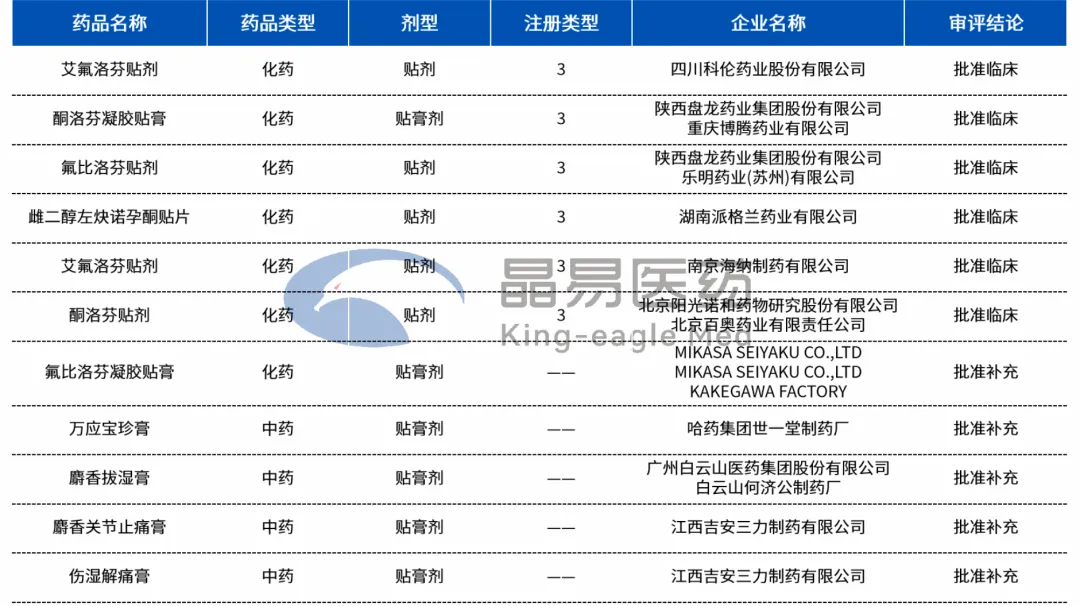
2026年1-2月,又有一批经皮给药制剂临床申请、补充申请获得批准。获批临床的品种中,共4款新药在列。

CKBA乳膏
1-2月获批临床的新药中,唯一一个1类创新药,来自江苏博创园生物。该产品并非首次申请临床,前几次适应症均有变更,最新的适应症调整为“拟用于治疗儿童非节段型白癜风”。
GenSci141软膏
由长春金赛药业申报,获批临床,属于2.2类新药,显示该企业在局部治疗领域的创新布局。
PTP23001透皮贴剂
重庆希尔安药业申报的2.2类新药,适应症为成人抑郁症,这是该产品首次申请临床。
湿润烧伤膏
一款用于治疗糖尿病足溃疡的中药2.3类新药,被改良对象为汕头美宝制药原有的同名独家品种,已上市多年。
此外,一些热门化药贴剂/贴膏剂仿制品种也获得批件。
雌二醇左炔诺孕酮贴片
由湖南派格兰药业申报,获批临床,适应症为治疗绝经期相关中重度血管舒缩症状,目前国内暂无任何仿制产品上市。
艾氟洛芬贴剂
共有2家企业的临床申请被批准,分别来自四川科伦、南京海纳。截至目前,国内共有7家企业拿到了该品种的IND批件。
氟比洛芬贴剂/凝胶贴膏
近几年非甾体抗炎药(NSAIDs)的热门外用产品。凝胶贴膏的原研日本三笠制药的补充申请被批准,另一企业的贴剂则获批临床。镇痛抗炎类外用制剂仍是研发热点。
综合2026年前2月的审评数据,经皮给药市场呈现出明显的特点。
经皮给药系统(TDDS)成为创新高地。无论是新药临床申请还是补充申请,贴剂/贴膏剂占据大量席位。而申请临床的化药3类品种全部为贴剂/贴膏剂。企业如四川科伦药业、陕西盘龙药业、湖南派格兰药业、乐明药业(苏州)等在TDDS领域的布局,显示经皮贴剂系统(TDDS)市场还在持续升温。
仿制药“红海”与改良型新药“蓝海”并存,外用药市场的竞争格局正在重塑。获批数据中“仿制”与“补充申请”数量可观,但无疑新药含金量更高。对于凝胶贴、热熔贴、透皮贴等剂型,由于存在较高的工艺壁垒和辅料壁垒,目前仍处于蓝海阶段。获批临床的企业,如能在后续研发中建立专利壁垒和工艺护城河,有望在未来一定时间内享受市场红利。
随着更多1类、2类新药进入临床阶段,经皮给药将在镇痛、脱发、皮肤病用药、两性用药等领域开启新一轮产品迭代与市场竞争,国内经皮给药市场将迎来一场由技术驱动的供给变革风暴。