本文将从关键临床试验设计策略、疗效与安全性、剂型创新的维度,解析酮洛芬贴剂的临床价值与市场潜力,揭示其在百亿级OA治疗市场中的突破性进展。
2019年,全球约5.3亿骨关节炎患者正在经历"沉默的疼痛风暴"!作为最常见的退行性肌骨系统疾病,我国骨关节炎标化患病率高于亚洲平均水平,庞大的人口基数与老龄化趋势,患者负担将进一步加重[1]。传统口服NSAIDs虽能短暂缓解症状,却暗藏致命隐患,36%的长期使用者可能面临消化道出血、心脑血管事件等系统性风险。酮洛芬贴剂通过局部透皮给药,显著降低全身暴露量,系统性风险显著降低,成为国内外权威指南推荐的镇痛药物。
1️⃣疗效显著:原研药酮洛芬贴剂(商品名MOHRUS®)III期临床研究显示[2],酮洛芬贴剂治疗慢性疼痛疾病的改善率达95%以上,与其他贴膏贴剂相比,镇痛效果更优,且起效快、持续时间长。
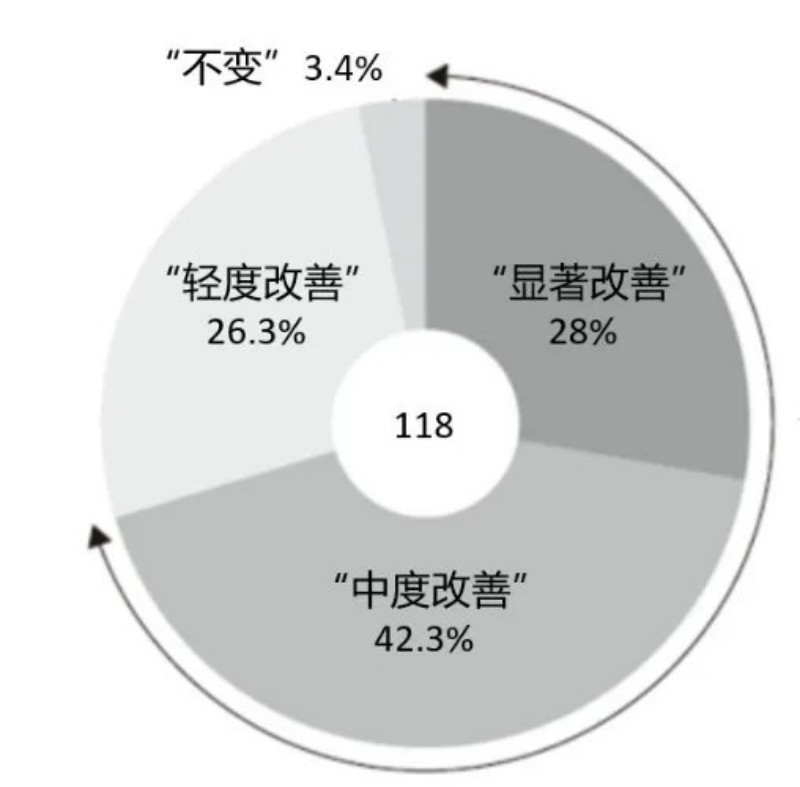
MOHRUS®治疗慢性疼痛疾病疗效的原研数据
2️⃣安全性突出:其安全性数据表明,主要不良反应为局部皮肤反应,如皮疹、瘙痒等,发生率低[2]。3️⃣适应症广泛:覆盖类风湿性关节炎、骨关节炎、肩周炎、肌肉痛、扭伤等多种疼痛场景,满足多科室临床需求。
市场前景:百亿蓝海与本土化机遇
1️⃣精准切入慢性疼痛刚需市场:慢性疼痛疾病的发病率不断上升,酮洛芬贴剂以局部给药方式实现非侵入性靶向镇痛,兼具高效与安全双重属性,直击患者“少副作用、便捷控痛”的核心诉求,市场渗透率持续提升。
2️⃣政策赋能OTC市场扩容:CDE批准酮洛芬贴剂转为非处方药,打破处方壁垒。患者可自主通过线上线下多渠道即时购药,尤其利好骨关节炎等需长期镇痛管理的患者群体,预计将带动国内零售终端销量爆发式增长。
3️⃣新兴市场与出口双轮驱动:亚太、拉美等新兴市场慢性病负担加重,本土化医疗需求激增,中国药企可依托产能与技术优势,同步开拓国内外增量市场。
临床路径:化药3类的临床设计核心
目前国内仅有贵州联盛药业有限公司的酮洛芬贴片独家上市,多家企业处于临床研发阶段,河北一品制药股份有限公司、内蒙古白衣制药股份有限公司、深圳珐玛易药品科技有限公司、湖南九典制药股份有限公司等企业提交了3类仿制药申请临床,均在审评审批中。此外,湖南九典制药股份有限公司已完成BE试验、III期临床试验,进度领先;河北一品制药股份有限公司BE试验进行中;深圳珐玛易药品科技有限公司III期临床试验进行中。
酮洛芬贴剂注册分类为化药3类,基于国家药监局发布的《皮肤外用化学仿制药研究技术指导原则》、《局部给药局部起效药物临床试验技术指导原则》等相关指导原则,3类仿制药需要验证其在中国人群中的有效性及安全性,同时考虑与参比制剂的生物等效性。目前登记公示公布的临床设计核心如下:
√湖南九典制药股份有限公司:通过PK-BE研究验证酮洛芬贴剂的生物等效性,III期临床试验采用阳性药/安慰剂平行对照的三臂试验,以已上市的LOXONIN®TAPE(洛索洛芬钠贴剂)为阳性对照,通过非劣效性设计验证疗效与安全性。
√深圳珐玛易药品科技有限公司:III期临床试验采用参比制剂(MOHRUS®)/安慰剂平行对照的三臂试验,通过等效性设计验证疗效一致性。

图源:摩熵医药数据库
参考国内同类产品大临床试验,酮洛芬贴剂的临床设计关键指标如下:√对照组:均设计安慰剂对照验证其疗效的优效性;阳性药选择已上市的产品如氟比洛芬凝胶贴膏、洛索洛芬钠凝胶贴膏等,或选择参比制剂验证其疗效的一致性;
√有效性指标:以VAS评分改善为核心,联合功能评价量表(WOMAC);
√安全性指标:重点评价局部皮肤刺激性、全身不良反应等;
√样本例数:400-500例。
目前已登记临床试验存在设计差异,其生物等效性评价包括药代动力学研究(PK-BE)、临床终点生物等效性研究,后续品种获批进展我们拭目以待。
关于晶易医药临床
晶易医药临床团队拥有1300+项BE/I~III期/IIT研究经验,尤其在透皮制剂临床研究领域具备突出的优势。团队不仅完成了多款外用非甾体抗炎药的等效性研究,更推动酮洛芬贴剂、酮洛芬凝胶贴膏、吲哚美辛凝胶贴膏等市场热门产品挺进III期临床。公司在临床进度上的领先优势,可以为酮洛芬贴剂的商业化加速铺路。
参考文献:
[1].WU Haotian,LIN Jianhao.Disease Burden and Harm of Osteoarthritis[J].Medical Journal of Peking Union Medical College Hospital,2025,16(1):5-12.
[2].MOHRUS®TapesL IF文件,久光製薬株式会社,2023年12月修订(第18版).


